天津市第一中心医院沈中阳、王树森研究组,北京大学、昌平实验室邓宏魁研究组与杭州瑞普晨创科技有限公司组成的研究团队,在国际上首次利用化学重编程诱导多能干细胞制备胰岛细胞,并移植给一名治疗1型糖尿病患者,该患者在移植后恢复了内源自主性、生理性的血糖调控,移植75天后完全稳定地脱离胰岛素注射治疗,目前疗效已稳定持续1年以上,实现了1型糖尿病的临床功能性治愈。

该照片拍摄于2023年6月30日患者手术后
摆脱胰岛素,实现功能性治愈
该成果于2024年9月25日晚发表于国际顶刊Cell,题为 Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patient 的研究论文。
糖尿病是全球范围内威胁人类健康的重大疾病之一,并且我国已成为全球糖尿病患病人数最多的国家。当前常用的治疗方法,如胰岛素注射、降糖药物,难以实现血糖的精准调控,导致多种并发症发生,严重影响患者的生活质量,甚至会危及生命。经过四十多年的临床积累,胰岛移植治疗糖尿病已取得较好的临床疗效,但人胰腺供体短缺的问题,严重限制了其广泛应用。
人多能干细胞(PSCs)制备的胰岛细胞为糖尿病移植治疗提供了新的来源。多能干细胞具有无限增殖的特性和分化成生物体所有功能细胞类型的能力,在细胞治疗、药物筛选和疾病模型等方向具有广泛的重要应用价值,是再生医学领域最具潜力的“种子细胞”。
研究团队成功地将人体细胞重编程为化学诱导的 PSCs (CiPSCs)。传统的 iPSCs 通过转录因子的遗传过表达从体细胞中产生,与之不同的是,从体细胞生成 CiPSC 采用非生物小分子化学物质作为重编程因子,这些化学物质易于制造和标准化、非基因组整合、可扩展和微调。这种方法为生成适用于治疗应用的人类 PSC(hPSC)提供了一种根本不同的途径。
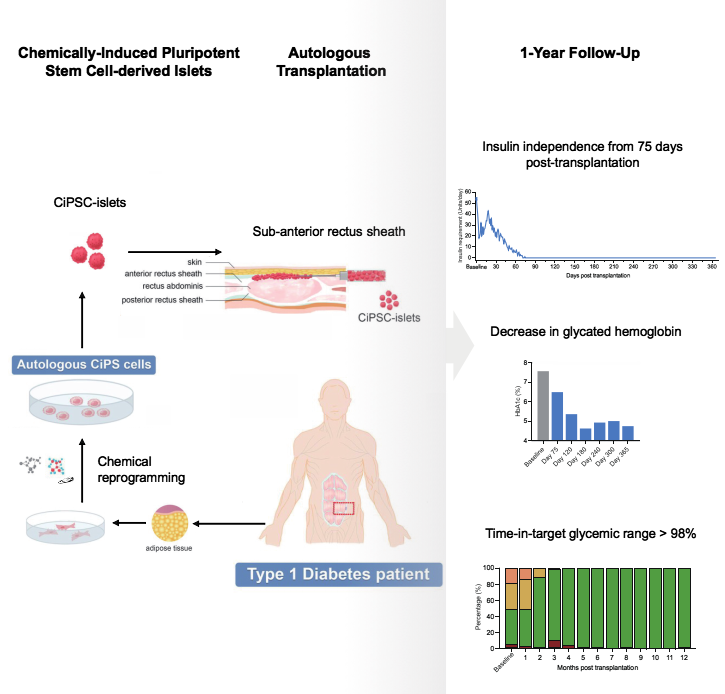
基于CiPS细胞治疗1型糖尿病的临床研究的示意图和治疗效果
该患者是一位病史长达11年的1型糖尿病病人,通过强化胰岛素治疗仍然不能有效控制血糖,为了治疗糖尿病,患者于2017年5月接受了胰腺移植手术,但一年后胰腺移植失功,并且患者群反应抗体呈现为强阳性,难以接受同种异体胰岛移植,然而自体细胞移植有可能解决这个难题。本临床研究移植前,患者血糖在目标血糖范围内的时间比例仅为43.18%,最近一年内多次发生严重低血糖,严重威胁患者的生命安全。2023年6月25日,患者接受了自体人CiPS细胞分化胰岛移植的治疗。
在该项人体 I 期临床试验(ChiCTR2300072200)的 1 年初步分析结果中,患者在移植 75 天后,完全稳定地脱离胰岛素注射治疗。移植后第 4 个月,患者的靶时血糖范围从基线值 43.18% 增加到 96.21%,同时伴有糖化血红蛋白下降。此后,患者血糖控制状态稳定,不使用外源胰岛素的情况下实现了超过 98% 的血糖 TIR,糖化血红蛋白在 5% 左右。1 年时,所有安全性和有效性临床终点均得到满足,患者未出现移植相关异常迹象;至论文发表时,患者已经超过 1 年无需胰岛素治疗。
多能干细胞技术治疗需要解决的一个关键问题,就是如何保证体内移植细胞的安全可控性。研究团队创新性将胰岛移植到腹直肌前鞘下部位,相对于传统的胰岛移植策略,该移植方案创伤小、操作简便、移植物易于长期追踪观察,并且必要时可进行移除。本研究首次在临床上实现了通过超声和核磁手段对移植物的有效监测,极大地提高了干细胞临床治疗研究过程的安全性和可控性。
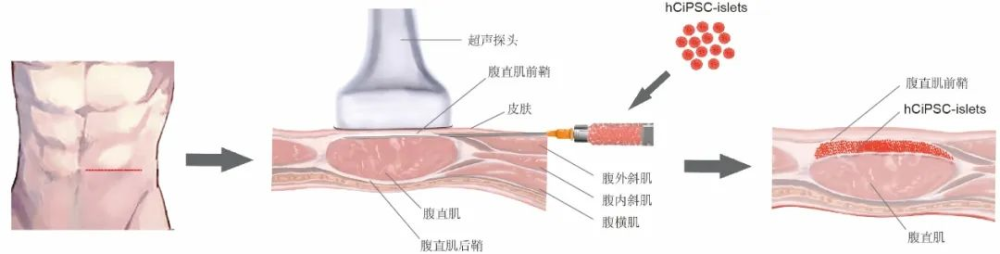
胰岛细胞腹直肌前鞘下移植的示意图
本研究利用人CiPS细胞制备的胰岛,建立了糖尿病的细胞治疗新途径,实现了临床功能性治愈糖尿病。更为重要的是,化学重编程技术制备的功能细胞在临床治疗疾病的成功,表明了化学重编程有望成为高效制备各种功能细胞类型的通用底层技术,为细胞治疗在重大疾病治疗上的广泛应用开辟了一条新的途径。
文章来源:天津市第一中心医院微信公众号
特别声明:本文文字、图片、 音频来源于网络资讯,仅供参考与学习,并非广告,若有侵权,请及时联系我们,我们将在第一时间处理。